Il Lichen Sclerosus in età pediatrica
di Vincenzo Bagnara
Il Lichen Sclerosus (LS) è una malattia infiammatoria cronica della cute mediata dai linfociti, che può interessare qualsiasi distretto cutaneo ma che mostra predilezione per l’area anogenitale sia nei maschi che nelle femmine.
La prima descrizione clinica dell’affezione si deve al dermatologo francese Hallopeau che, nel 1887, le diede il nome di “Lichen plan atrophique”. Nel 1892 Darier descrisse gli aspetti istologici della malattia e la denominò “Lichen plan scléroux”.
Avendo constatato che l’atrofia non risultava sempre istologicamente dimostrabile, nel 1976 Friedrich propose di eliminare l’aggettivo “atrophicus” lasciando solo la definizione di Lichen Sclerosus (LS).
La forma genitale maschile del LS fu descritta dettagliatamente per la prima volta nel 1928 da Stuhmer che propose il nome di “Balanitis (infiammazione cronica del glande) Xerotica (aspetto sclerotico, secco della lesione) Obliterans (associazione occasionale con l’endoarterite obliterante)” o, secondo il suo acronimo, BXO.
Da allora le due denominazioni ed i corrispondenti acronimi LS e BXO sono stati usati indifferentemente e, comunque, la prima descrizione della BXO nel bambino risale solo al 1962 in un case report di Catterall e Oates.
La differente definizione di uno stesso processo patologico e, quindi, la possibilità di ingenerare confusione, ha spinto nel 1976 “The International Society for the Study of Vulvovaginal Disease” e, nel 1995, “The American Academy of Dermatology” ad adottare la definizione di “Lichen Sclerosus” per definire questa patologia in maniera univoca in entrambi i sessi ed in tutte le sue forme e localizzazioni.
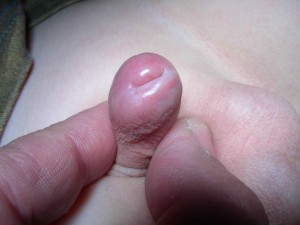
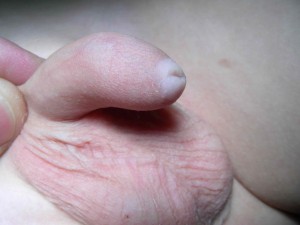
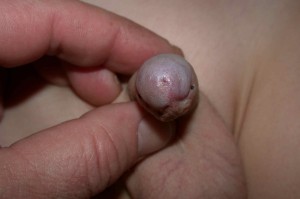
Considerato inizialmente come occasionale, il LS nel maschio giovane è oggi riconosciuto come causa di fimosi (Figg. 1,2) e di stenosi del meato uretrale (Figg. 3,4).
Il problema, semmai, è che a tutt’oggi troppo spesso il LS non viene clinicamente riconosciuto e, quindi, non viene trattato. Infatti, la reale incidenza del LS è probabilmente sottostimata nella popolazione generale ed in particolare in quella maschile pediatrica.
Studi prospettici su bambini con indicazione al trattamento chirurgico della fimosi hanno documentato un’incidenza di BXO compresa tra il 10% ed il 95%. In particolare, uno studio su 1.178 ragazzi affetti da fimosi e sottoposti a circoncisione ha dimostrato nel 40% dei casi la presenza di LS all’esame istologico con l’incidenza più alta tra 9 e 11 anni.
Il LS è più comune nella razza caucasica; è più frequente nella donna con un rapporto F/M variabile da 6:1 a 10:1. Tuttavia, la sua manifestazione è più precoce nei maschi, ed è stato descritto negli adolescenti e nei bambini sin dall’età di un anno.
Nel LS non sono stati evidenziati veri fattori di rischio e la vera etiologia è sconosciuta.
A tal proposito sono state proposte diverse teorie ed ipotesi etiopatogenetiche:
– Teoria autoimmune, Meccanismi molecolari e Fattori genetici: associazione con diabete, vitiligo, alopecia;
– Infezione: alta incidenza di HPV riscontrata in pazienti pediatrici maschi con LS genitale;
– Influenza ormonale: la più alta incidenza di LS nelle donne si osserva nei periodi di fisiologica riduzione del livello degli estrogeni;
– Fattori irritativi locali: fenomeno di Koebner (induzione di patologia cutanea in aree sottoposte a stimoli meccanici prolungati, anche lievi, che siano in grado di ledere o traumatizzare i piccoli vasi degli strati superficiali della cute).
Nondimeno, l’evidenza clinica comune indica che il LS nel maschio è dovuto, nella maggioranza dei casi, ad occlusione cronica del recesso balano-prepuziale con conseguente esposizione cronica all’urina di un epitelio suscettibile.
Infatti, la condizione:
– non si osserva mai negli uomini circoncisi alla nascita;
– è spesso associata a traumi, piercing genitale ed anomalie anatomiche (es. ipospadia);
– recidiva frequentemente negli innesti;
– non si manifesta a livello del perineo (contrariamente alla donna, il perineo del maschio non è mai esposto cronicamente all’azione irritazione dell’urina, esclusi casi particolari e rarissimi, ad es., di ipospadia) ma interessa il glande ed il prepuzio.
Il LS può avere un andamento cronico e progressivo o acuto ed aggressivo. Molti pazienti possono rimanere asintomatici per lunghi periodi. Nel maschio, inoltre, la localizzazione genitale del LS rispetto ad altre regioni supera il rapporto di 5:1. Depasquale in uno studio retrospettivo su 522 pazienti ha riscontrato che la malattia era limitata al prepuzio ed al glande nel 57% dei casi; al meato uretrale nel 4%, con il 20% che presentava un interessamento dell’uretra. La fimosi è il quadro di presentazione del LS più comune nel maschio in età pediatrica.
L’aspetto clinico macroscopico dell’LS rileva inizialmente una colorazione bianco-grigiastra del glande e/o del prepuzio (una placca sclerotica, bianca disposta sull’intera circonferenza della parte distale del prepuzio è presente nel 71-100% dei pazienti). La progressione della malattia sul frenulo e sul prepuzio può portare a fimosi con prepuzio non retraibile, cute prepuziale assottigliata e fragile e placce sclerotiche. Con il tempo la cute coinvolta può diventare anelastica con possibili lacerazioni e creazione di ragadi radiali.
I sintomi più frequenti possono essere suddivisi in:
– soggettivi: prurito, dolore, bruciore;
– legati alla stenosi del meato: disuria e mitto ipovalido; sintomi ostruttivi; mitto deviato o bifido;
– legati al restringimento ed alla flogosi del prepuzio: “ballooning” perminzionale; difficoltà a retrarre il prepuzio con possibile fusione al glande; lacerazioni in corso di igiene o di attività sessuale.
Nonostante l’aspetto clinico caratteristico, il LS genitale spesso non viene riconosciuto. Bale ha rilevato che i chirurghi del suo gruppo, dopo avere fatto esperienza con il primo o i primi due casi nei quali si fosse avuta conferma istologica dell’affezione, erano capaci di riconoscere clinicamente il LS in almeno l’80% dei pazienti. Questo dato è corroborato dalla nostra esperienza tanto che, su una casistica di 18 pazienti nei quali avevamo il sospetto clinico di LS abbiamo ricevuto conferma istolopatologica in 17 casi, pari al 94%.
Gli obiettivi del trattamento del LS sono: alleviare i sintomi; prevenire le lesioni cancerose; risolvere o migliorare i problemi urinari e sessuali.
Il trattamento medico del LS prevede l’uso locale di steroidi mentre più raramente è necessario il ricorso a terapie ormonali e sistemiche. Il trattamento chirurgico del LS, invece, include la circoncisione, la meatoplastica e l’uretroplastica.
L’incidenza del LS nel bambino è superiore a quanto riferito in precedenza ma la diagnosi è posta raramente dai pediatri. L’evoluzione imprevedibile della malattia giustifica la necessità di un riconoscimento precoce e la sua segnalazione allo specialista perché il trattamento tardivo comporta maggiori danni per il glande, il meato uretrale, l’uretra e, quindi, la possibilità di importanti e non sempre risolutivi interventi di chirurgia ricostruttiva.
L’uso topico di corticosteroidi è di beneficio nella fase acuta del LS (riduce il prurito e l’arrossamento) e nel postoperatorio come adiuvante nel trattamento del LS. È auspicabile la conferma istologica precoce della lesione ed il paziente e/o i genitori devono essere bene informati sul decorso cronico della malattia e la sua associazione con il tumore del pene. Il LS è, infatti, una lesione precancerosa e l’incidenza di neoplasia tra i pazienti con LS varia dal 2.3 all’8.4%. Per questo motivo i pazienti con LS dovrebbero seguire un attento follow-up ed ogni lesione sospetta dovrebbe essere sottoposta a biopsia.