Il “criptorchidismo” (dal greco κρυπτος, nascosto, e όρχυς, testicolo), è la mancata discesa di uno o di entrambi i testicoli nello scroto (Foto 1).
L’abbozzo testicolare si forma in utero a livello del polo inferiore del rene. Da questa posizione il testicolo migra lungo il tragitto che, attraversando il canale inguinale, lo porterà al fondo della borsa scrotale nel corso del settimo mese di gravidanza. L’arresto di questa migrazione, a qualsiasi livello avvenga, determina il criptorchidismo (Fig 1).
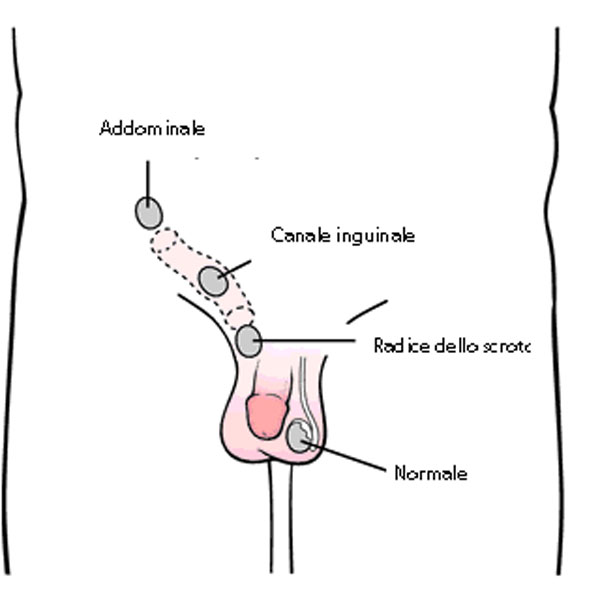
Fig 1 – Principali localizzazioni del testicolo criptorchide. La linea tratteggiata evidenzia il canale inguinale.
In alcuni casi il testicolo devia dal suo tragitto raggiungendo una meta differente: in questo caso si parlerà di testicolo ectopico (Foto 2).
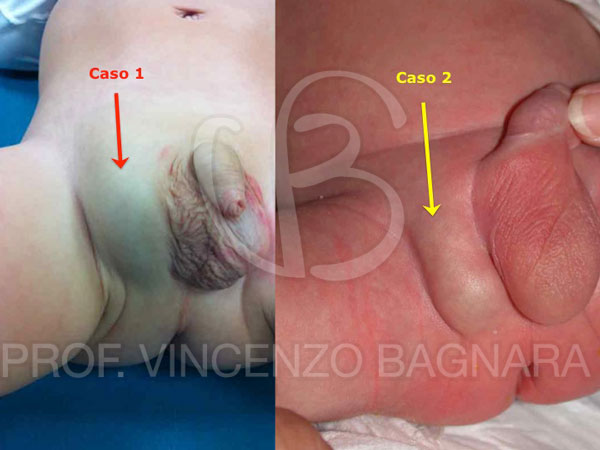
Foto 2 – Testicolo destro posto lateralmente allo scroto verso la regione femorale (Ectopia femorale)
La necessità del trattamento del criptorchidismo è connesso a problemi quali l’infertilità (anche nei pazienti con criptorchidismo monolaterale), l’aumento della frequenza di neoplasie del testicolo, l’aumento del rischio di torsione del testicolo e di traumi contro l’osso pubico, i possibili risvolti psicologici legati ad uno “scroto vuoto”. La terapia è il riposizionamento chirurgico del testicolo nello scroto (orchidopessi) ma, nonostante questo, possono comunque osservarsi problemi a lungo termine come la sterilità, l’infertilità e lo sviluppo di tumori maligni.
Epidemiologia
Il 3% dei maschi nati a termine e fino al 45% di quelli prematuri hanno un criptorchidismo. Questa percentuale scende all’ 1% dai 3 mesi di età. Ci sono due picchi per il rilevamento di criptorchidismo: alla nascita ed a 5-7 anni di età. Quest’ultimo gruppo è rappresentato probabilmente da quei pazienti con criptorchidismo basso che diventa più evidente durante la crescita in altezza del corpo (“ascending testis”). Un criptorchidismo bilaterale si osserva nel 10% dei pazienti criptorchidi mentre l’anorchia unilaterale nel 5%. Possibili fattori di rischio per il criptorchidismo possono essere l’età materna avanzata e l’obesità, il diabete o il consumo di bevande contenenti cola durante la gravidanza, una storia familiare di criptorchidismo, la prematurità, la presentazione podalica e la nascita di basso peso o piccolo per età gestazionale.
Fisioplatologia
La discesa dei testicoli normali avviene in utero durante il settimo mese di gestazione. La maggior parte dei testicoli scende spontaneamente fino ai 3 mesi di età, probabilmente a causa dell’impennata di gonadotropina (ormone luteinizzante (LH) ed ormone follicolo – stimolante (FSH)) che avviene a circa 60-90 giorni di vita e che è responsabile della maturazione delle cellule germinali.
Etiologia
Di tutti i bambini con criptorchidismo, il 4% dei loro padri ed il 6-10% dei loro fratelli hanno la stessa malformazione. Anche se è proponibile una causa genetica, nel criptorchidismo l’eziologia più probabile è poligenica e multifattoriale. Schnack, rivedendo le nascite di oltre un milione di maschi ha verificato che i rapporti di rischio per criptorchidismo erano di 10,1 nei gemelli, di 3,5 nei fratelli e di 2,3 nella prole dei padri che avevano un criptorchidismo. I fattori ereditari, quindi, sono presenti ma hanno una influenza moderata sul rischio di criptorchidismo. Sembrerebbe inoltre che anche i fattori materni in utero sono importanti per il rischio di criptorchidismo.
Esame clinico
Il testicolo può essere collocato nella parte alta dello scroto, a livello dell’anello inguinale superficiale (vicino il tubercolo pubico), nel contesto del canale inguinale, o può non essere palpabile (20% dei casi). Il paziente deve essere esaminato anche seduto nella posizione con “gambe a rana” con le mani riscaldate e controllare la dimensione, la posizione e la consistenza del testicolo disceso controlaterale. Il testicolo può essere ritenuto anche in addome. In questo caso non è possibile apprezzarlo alla visita e, pertanto, viene definito come testicolo “non palpabile”. Inoltre, il testicolo può essere ectopico quando si trova al di fuori del suo normale sentiero di discesa come ad esempio a livello della regione femorale o di quella perineale (Foto 2).
Nel paziente con criptorchidismo monolaterale (e testicolo palpabile o non palpabile), o nel paziente con criptorchidismo bilaterale e un testicolo palpabile, non è necessario nessun approfondimento diagnostico. Il paziente con testicoli entrambi non palpabili, invece, dovrebbe essere sottoposto ad una valutazione cromosomica ed endocrinologica, così come il paziente con criptorchidismo mono o bilaterale ed ipospadia prossimale. Se il paziente ha i testicoli non palpabili bilateralmente ed è inferiore a tre mesi di età, la determinazione del testosterone, dell’ormone follicolo – stimolante (FSH), del fattore inibente Mulleriano (MIF) e dell’ormone luteinizzante (LH) determinerà se i testicoli sono presenti. Nei neonati con testicoli entrambi non palpabili, se è presente anorchia, non si verificherà l’impennata di testosterone postnatale. Dopo l’età di tre mesi, la stimolazione con gonadotropina corionica umana determinerà, se i testicoli sono presenti, un aumento del testosterone sierico. Una mancata risposta alla stimolazione con gonadotropina corionica umana in combinazione con elevati livelli di LH ed FSH è coerente con l’anorchia.
Il solo esame clinico da parte di un urologo pediatra esperto è sufficiente a verificare la presenza e la localizzazione di un testicolo criptorchide nell’84% dei casi. A volte può dimostrarsi utile l’Ecografia (Foto 3) mentre la TAC e la risonanza magnetica (RMN) trovano indicazione raramente. Anche le decisioni terapeutiche sono prese generalmente solo sulla scorta dell’esame clinico.
La diagnosi differenziale va posta innanzitutto con:
– i testicoli retrattili o “in ascensore”. In questi casi il testicolo si trova dislocato in alto
non per una mancata discesa ma per la contrazione del muscolo cremastere che trazionando sul funicolo attrae verso l’alto il testicolo. Anche in questo caso il semplice esame clinico da parte dello specialista chiarisce la diagnosi;
– il testicolo atrofico o “vanisching testis” può trovarsi ovunque lungo il percorso che la gonade segue per raggiungere lo scroto (Foto 4, 5).
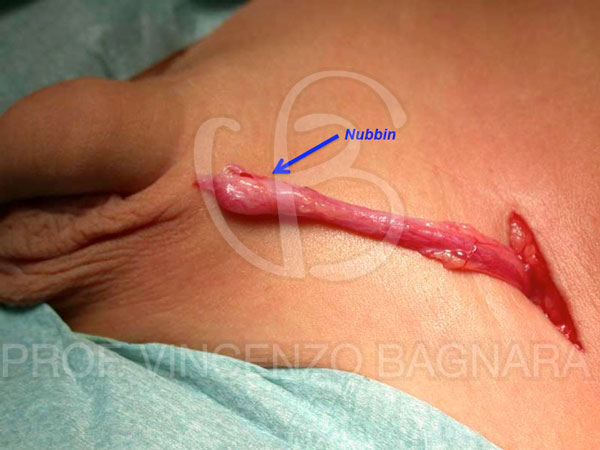 Foto 4 – Atrofia del testicolo di sinistra. Dopo l’isolamento del funicolo è riscontrabile distalmente solo una struttura definita “nubbin” (vedi testo)
Foto 4 – Atrofia del testicolo di sinistra. Dopo l’isolamento del funicolo è riscontrabile distalmente solo una struttura definita “nubbin” (vedi testo)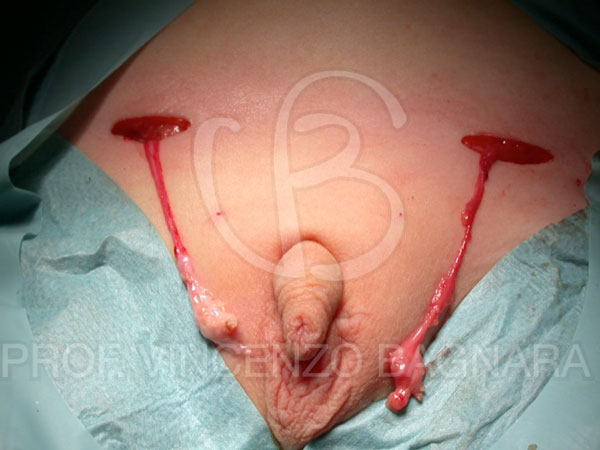 Foto 5 – Atrofia testicolare bilaterale. Da notare come anche entrambi i funicoli siano estremamente ipoplasici.
Foto 5 – Atrofia testicolare bilaterale. Da notare come anche entrambi i funicoli siano estremamente ipoplasici.Questo aspetto si pensa possa essere dovuto a fatti ischemici. Il testicolo disceso controlaterale può essere ipertrofico (ipertrofia compensatoria). Comunque, l’80% dei testicoli non palpabili sono presenti in addome o lungo il canale inguinale.
Un bambino con entrambi i testicoli non palpabili dovrebbe essere sottoposto a valutazione endocrinologica per escludere un disturbo dello sviluppo sessuale (DSD o intersex) o l’anorchia. Infine, il criptorchidismo associato ad ipospadia si associa nel 30- 40% dei casi a DSD.
Trattamento
Il trattamento ormonale dei pazienti con criptorchidismo è stato ampiamente utilizzato in Europa per indurre la discesa del testicolo. Il trattamento è più efficace nelle ritenzioni basse. Alcuni meta-analisi concludono che l’ efficacia della terapia ormonale nel criptorchidismo primario è inferiore al 20%. D’altra parte oggi si scoraggia l’uso della terapia ormonale per la cura del criptorchidismo che invece può essere utile dopo intervento di orchidopessi per migliorare la qualità dello sperma in pazienti ad alto rischio.
Chirurgia
gli obiettivi di ricollocare i testicoli nello scroto sono:
– evitare ulteriori danni termici;
– trattare il sacco erniario associato (isolamento e chiusura del dotto peritoneo- vaginale);
– evitare la torsione del testicolo ed i traumi contro il pube;
– raggiungere un buon risultato estetico (evitando gli effetti psicologici legati ad uno scroto vuoto);
– consentire l’autopalpazione dei testicoli per la prevenzione dei tumori.
L’intervento standard di orchidopessi è quello di Shoemaker. Questa tecnica prevede un’incisione inguinale, la localizzazione e l’isolamento del testicolo e quindi del funicolo spermatico, la sezione del gubernaculum, la separazione di vasi sanguigni e del deferente dal dotto peritoneo-vaginale e la chiusura dello stesso a livello dell’anello inguinale interno. Un’ulteriore allungamento del funicolo può essere ottenuto liberando i vasi nel retroperitoneo. Il testicolo così mobilizzato viene quindi collocato e fissato in una tasca sottodartoica realizzata previa incisione dello scroto omolaterale.
ln alcuni casi è possibile eseguire l’orchidopessi con un unico approccio transcrotale (intervento di A. Bianchi). Altre tecniche chirurgiche come quella di Fowler-Stephens sono utilizzate in casi selezionati come per testicoli intraddominali e/o con funicolo spermatico molto corto.
Tra le possibili complicanze sono da segnalare la retrazione del testicolo o l’atrofia (0- 2%), e la comparsa di un’ernia (2-3%).
L’esplorazione chirurgica per un testicolo non palpabile può essere eseguita attraverso un’incisione inguinale estesa, o un’incisione addominale, o con laparoscopia diagnostica. All’esplorazione, i risultati più probabili sono testicolo intraddominale o “che fa capolino -peeping testis-” attraverso l’anello inguinale interno (25-50%), o vanisching testes distalmente all’anello inguinale interno (15-40%), o funicolo spermatico con vasi e deferente che entrano attraverso l’anello interno con un testicolo vitale non palpato a causa delle dimensioni del testicolo o dell’habitus del corpo del paziente (es. paziente obeso).
L’agenesia dei testicoli è un evenienza estremamente rara. Anche se controverso, dovrebbe essere preso in considerazione la fissazione del testicolo solitario per proteggerlo contro il rischio teorico di torsione.
In particolare, alcuni chirurghi raccomandano la fissazione del testicolo scrotale controlaterale allorquando venga riscontrato un “nubbin*” all’interno dello scroto (Foto 4, 5).
* Tessuto fibroso derivato dalla degenerazione, per compromissione vascolare, del testicolo. È ricco in depositi di emosiderina ed è quasi sempre presente l’epididimo con il deferente.
Infertilità
La chirurgia non può guarire la mancata maturazione del testicolo ritenuto, ma può prevenire ulteriori danni causati dal trauma termico. Infatti, il testicolo criptorchide presenta spesso una ipodisplasia congenita dove la deconnessione didimo- epididimaria rappresenta l’aspetto macroscopico più evidente (Foto 6).
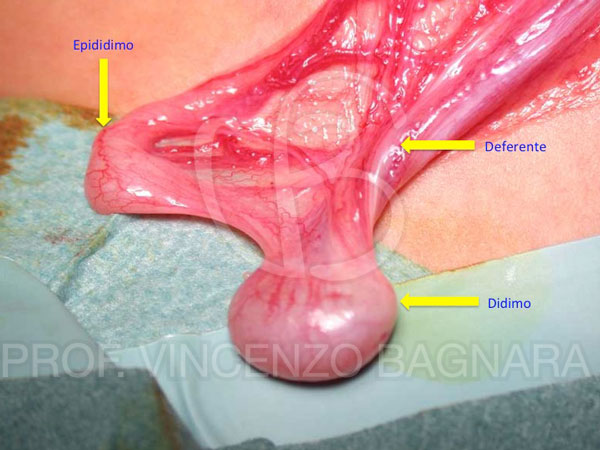 Foto 6 – Ipodisplasia in criptorchidismo sinistro. A parte l’ipoplasia è presente una deconnessione didimo-epididimaria completa
Foto 6 – Ipodisplasia in criptorchidismo sinistro. A parte l’ipoplasia è presente una deconnessione didimo-epididimaria completaL’arresto dello sviluppo degli spermatogoni è un riscontro comune nei testicoli criptorchidi ed è conosciuto da oltre 40 anni e ciò aumenta il rischio di infertilità. Così come è anche descritta una riduzione delle cellule di Leydig nel testicolo criptorchide rispetto al controlaterale tanto più marcata quanto più aumenta l’età dell’orchidopessi. Questo quadro può alterare la fertilità (numero di spermatozoi) ma non necessariamente la paternità cioè la possibilità di diventare padre. Infatti, il 90% dei ragazzi con criptorchidismo unilaterale e il 65% con criptorchidismo bilaterale raggiungerà la paternità. I pazienti interessati a valutare il rischio di infertilità possono eseguire l’esame dello sperma all’età di 18 anni.
Prognosi
Questo è un campo controverso e la percezione del rischio è cambiata nel corso degli anni. Così, da un rischio che in passato era stimato circa 40 volte superiore, attualmente la stima è di circa 6 volte nel criptorchidismo unilaterale e 10 volte in quello bilaterale. Tuttavia, il calcolo del rischio suggerisce che su 100 bambini trattati chirurgicamente, uno potrebbe sviluppare un tumore maligno durante l’età adulta.
Dati recenti suggeriscono che il rischio di degenerazione maligna può essere 2-6 volte maggiore negli uomini sottoposti a orchidopessi dopo la pubertà, rispetto a quelli operati precocemente. L’orchiectomia è l’opzione migliore per l’età post-puberale e fino ai 50 anni perchè le gonadi hanno una scarsa potenzialità fertile ed un aumento del rischio di cancro. Il trattamento conservativo, invece, è raccomandato negli uomini over 50 in quanto il rischio di cancro oltre questa età non è mai stato definito. Infine, il tumore maligno che si sviluppa su un testicolo criptorchide è frequentemente un seminoma (74%), mentre dopo orchidopessi i due terzi delle neoplasie sono non-seminoma. Circa il 15% dei tumori nascono nel testicolo controlaterale normalmente disceso.
Alcuni pazienti affetti da criptorchidismo sono a più alto rischio di tumore (sindrome di Prune Belly, genitali ambigui, anomalie del cariotipo). Dopo l’intervento di orchidopessi i pazienti vengono seguiti per un periodo di 12-24 mesi per controllare dimensione e posizione dei testicoli. Successivamente sono ricontrollati alla pubertà anche per spiegare la tecnica e la necessità di eseguire mensilmente l’autopalpazione per il riconoscimento precoce del tumore al testicolo. Nei pazienti con testicoli retrattili è consigliabile un follow-up annuale fino alla pubertà, in quanto circa il 5% diverrà realmente criptorchide e richiederà un trattamento chirurgico (Ascending testis syndrome).